Thermische Energie kann mittels chemischer Reaktionen gespeichert werden. Dem Laien wesentlich geläufiger ist jedoch die Speicherung elektrischer Energie über chemische Reaktionen, wie sie z.B. beim Auto-Akku stattfindet. Während eine galvanische Zelle oder eine Batterie (dies ist die Hintereinanderschaltung mehrerer galvanischer Zellen) ihre chemische Energie nur einmal in elektrische Energie wandeln können und dann entsorgt werden müssen, sind Akkumulatoren wieder aufladbar. Zur Zeit noch am weitesten verbreitet sind die Bleiakkumulatoren, bei denen im Prinzip zwei Bleiplatten in verdünnte Schwefelsäure getaucht werden. Ein Nachteil der Bleiakkus ist ihre hohes Gewicht und damit verbunden ihre relativ niedrige Energiedichte bezüglich der Masse. Für spezielle Anwendungen (z.B. Akku für Laptop oder MP3-Player) hat man daher Akkus mit anderen Elektroden und Elektrolyten entwickelt, die sich durch eine höhere Energiedichte bezüglich der Masse bzw. bezüglich des Volumens auszeichnen. Wenn dich der Aufbau dieser neueren Akkus interessiert, so kannst du dich in der Schrift der Firma Varta (Adresse: http://static.varta-consumer.de/uploads/grs_welt_der_batterien.pdf) schlau machen.
Die folgende Abbildung stellt die Energiedichte verschiedener Akkumulatoren bezüglich des Gewichts und des Volumens dar. Man sieht, dass der preislich günstige Blei-Akku für anspruchsvollere Einsatzmöglichkeiten wie z.B. beim Elektroauto nicht gut abschneidet.

Energiespeicher Wasserstoff
Wasser (H2O) ist auf der Erde in Hülle und Fülle vorhanden, es ist ungiftig und die Bindung zwischen den zwei Wasserstoffatomen (H) und dem Sauerstoffatom (O) sehr stabil. Wasser kann nur unter Energieaufwand in Wasserstoff und Sauerstoff getrennt werden. Man ist heute der Meinung, dass der Wasserstoff in der Zukunft einen sehr wichtigen Energiespeicher darstellen wird.
Wasserstoffelektrolyse
Zur Erzeugung von Wasserstoff gibt es mehrere Verfahren. Im Folgenden wird die Wasserstoffelektrolyse, bei der elektrische Energie für den Trennvorgang eingesetzt wird, näher behandelt.
Wasserelektrolyse - PEM-Verfahren
- Kernstück dieses Elektrolyseverfahrens ist eine Kunststoffmembran, welche für H+-Ionen (Protonen) durchlässig ist (proton exchange membran).
- Die Membran ist beidseitig mit einem Katalysator (Platin bzw. Iridium) beschichtet.
- Auf der Anodenseite zerlegt der Katalysator das Wasser in Sauerstoff, Protonen und Elektronen.
- Nur die Protonen können durch die Membran gelangen (diffundieren).
- Die Elektronen, die den Weg über die elektrische Energiequelle nehmen vereinigen sich an der Kathode mit den Protonen zu Wasserstoff.
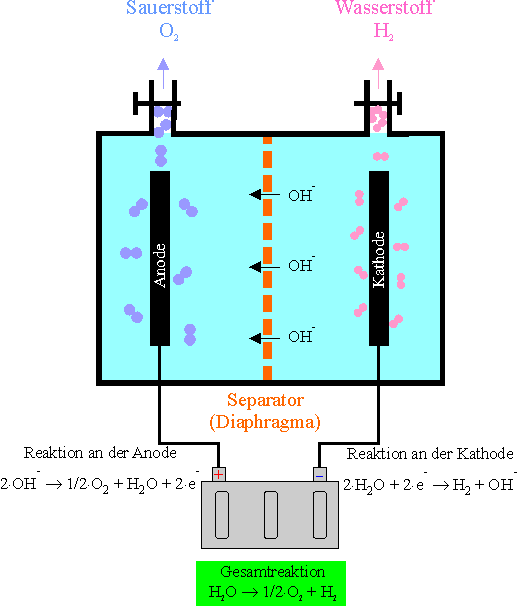
Das PEM-Verfahren wird z.Z. in kleineren Apparaturen eingesetzt, während für große Wasserstoffmengen die schon sehr ausgereifte klassische Elektrolyse ihre Anwendung findet.
Eine wirtschaftliche Wasserelektrolyse setzt eine billige elektrische Energie voraus, die nur an manchen Orten der Erde (z.B. Norwegen) zur Verfügung steht. Wenn du an weiteren Verfahren (die noch z.T. in der Erprobung sind) interessiert bist, dann kannst du dich auf den folgenden Seite informieren:
- http://www.innovation-brennstoffzelle.de/ (klicke dazu das Thema "Wasserstoff" an.
- http://www.diebrennstoffzelle.de/wasserstoff/herstellung/index.shtml


