Hinweis: Die Informationen zu diesem Artikel stammen von Dr. Walter Bube.
Brennstoffzellen wandeln mit hohem Wirkungsgrad die Energie von chemischen Oxidationsreaktionen direkt in elektrische Energie um, als Nebenprodukt entsteht auch Wärme. Es gibt viele Typen von Brennstoffzellen, die sich durch ihren Aufbau und den eingesetzten Energieträger unterscheiden und die für verschiedene Anwendungen und Leistungsbereiche optimiert sind.
Aufbau und Funktionsweise einer Brennstoffzelle
Das Prinzip der Umwandlung chemischer Energie in elektrische Energie soll an einer PEM (Polymer Elektrolyt Membran) Brennstoffzelle erklärt werden, die mit Wasserstoff und Sauerstoff arbeitet. Im Innern einer PEM-Brennstoffzelle reagiert Wasserstoffgas mit Sauerstoff, als Reaktionsprodukt entsteht Wasser. Dabei wird ein Großteil der Reaktionsenergie direkt in elektrische Energie verwandelt. Die Animation in Abb. 1 zeigt den prinzipiellen Aufbau und die Funktionsweise einer PEM-Brennstoffzelle.
Die Brennstoffzelle besteht aus zwei gasdurchlässigen Elektroden, der Anode und der Kathode, die durch eine gasdichte Membran voneinander getrennt sind. Beide Elektroden sind mit einem Platinkatalysator beschichtet, der die Reaktionen an den Elektroden unterstützt:
An der Anode werden vom Wasserstoffmolekül negativ geladene Elektronen abgetrennt. Die dabei zurückbleibenden positiv geladenen Protonen können die Ionen leitende Membran (Elektrolyt) durchqueren und wandern in Richtung Kathode. Die Elektronen gelangen über den äußeren Stromkreis dorthin. An der Kathode nehmen die Sauerstoffmoleküle Elektronen auf und vereinigen sich mit den Protonen zu Wassermolekülen.
Der Betrieb der Brennstoffzelle ist umweltschonend, weil als Endprodukte neben der nutzbaren elektrischen Energie lediglich Wasser und Wärme entstehen. Allerdings ist es für die ökologische Gesamtbilanz entscheidend, wie der Wasserstoff gewonnen und transportiert wird (Energieaufwand, Emission von Schadstoffen). Die Brennstoffzelle kann man als Umkehrprozess zur Elektrolyse sehen, wo Wasser mit Hilfe von elektrischer Energie in die gasförmigen Bestandteile Wasserstoff und Sauerstoff zerlegt wird.
Chemisch betrachtet, laufen in der Brennstoffzelle folgende Reaktionen ab:
Anode: \(2 \cdot {{\rm{H}}_{\rm{2}}} \to 4 \cdot {{\rm{H}}^ + } + 4 \cdot {e^ - }\)
Kathode: \({{\rm{O}}_{\rm{2}}} + 4 \cdot {{\rm{H}}^ + } + 4 \cdot {e^ - } \to 2 \cdot {{\rm{H}}_{\rm{2}}}{\rm{O}}\)
Gesamtreaktion: \(2 \cdot {{\rm{H}}_2} + {{\rm{O}}_2} \to 2 \cdot {{\rm{H}}_{\rm{2}}}{\rm{O}}\)
Hinweis: Die folgende Tabelle soll nur einen Eindruck von der Vielzahl der verschiedenen Brennstoffzellentypen vermitteln. Man sollte vorallem das Grundprinzip der Arbeitsweise einer Zelle verstehst.
| Typ | Anodengas | Kathodengas | Elektrolyt | Arbeitstemperatur | Leistungsbereich | Zellen-Wirkungsgrad |
|---|---|---|---|---|---|---|
| Alkalische Brennstoffzelle AFC |
Wasserstoff | Sauerstoff | Kalilauge | 20°C - 90°C | bis - 100 kW | 60% - 70% |
| Membranbrennstoffzelle PEMFC |
Wasserstoff | Luftsauerstoff | Polymer-Membran | 20°C - 80°C | bis - 500 kW | 50% -70% |
| Direkt-Methanolbrenn- stoffzelle DMFC |
Methanol | Luftsauerstoff | Polymer-Membran | 20°C -130°C | bis - 100 kW | 20% - 30% |
| Phosphorsäure-Brenn- stoffzelle PAFC |
Wasserstoff Erd- bzw. Biogas |
Luftsauerstoff | Phosphorsäure | 160°C - 220°C | bis 10 MW | 55% |
| Carbonatschmelzen-Bren- stoffzelle MCFC |
Erd-, Kohle- Biogas |
Luftsauerstoff | Alkalicarbonat- schmelzen |
620°C - 660°C | bis 100 MW | 65% |
| Oxidkeramische Brenn- stoffzelle SOFC |
Erd-, Kohle- Biogas |
Luftsauerstoff | Yttriumstabilisiertes Zirkonoxid |
800°C - 1000°C | bis 100 MW | 60% - 65% |
Wirkungsgrad von Brennstoffzellensystemen
Der Wirkungsgrad einer Brennstoffzelle für die Wandlung in elektrische Energie bewegt sich abhängig vom Betriebszustand, von der Bauweise und der Anwendung zwischen 35% und 65%. Weil Brennstoffzellen chemische Energie direkt in elektrische Energie umwandeln, ersparen sie den umständlichen und verlustreichen Umweg über Turbine und Generator, der in konventionellen Kraftwerken nötig ist. Dort entweichen bis zu zwei Drittel der eingesetzten Energie als Abwärme über Kühlwasser und Kamin – eine Verschwendung, die aber aus physikalischen Gründen bei thermodynamischen Maschinen (Automotor, Dampfmaschine, Dampfturbine, Gas- und Dampf-Kraftwerk) nicht zu vermeiden ist. Da Brennstoffzellen grundsätzlich anders arbeiten, wandeln sie mehr als die Hälfte der eingesetzten Energie in Elektrizität um. Damit übertrifft ihr Wirkungsgrad den konventioneller Kraftwerke, die Strom über den Umweg mechanischer Arbeit erzeugen. Die Grafik vergleicht typische Wirkungsgrade verschiedener Energiewandlersysteme. Kann auch die anfallende Wärme z.B. für Heizungen genutzt werden, ist der Gesamtwirkungsgrad nochmals erhöht.
Treibstoffe
Man kann Brennstoffzellen entweder mit reinem Wasserstoff betreiben oder mit einer Reihe von Wasserstoffverbindungen, etwa mit Erdgas, Biogas, Methanol oder Benzin. Diese Stoffe müssen aber in einem vorgeschalteten "Reformer" erst chemisch aufbereitet werden. Dabei entstehen chemische Verbindungen, die Kohlenstoff enthalten und bei der Verbrennung zu Kohlendioxid zum Treibhauseffekt beitragen.
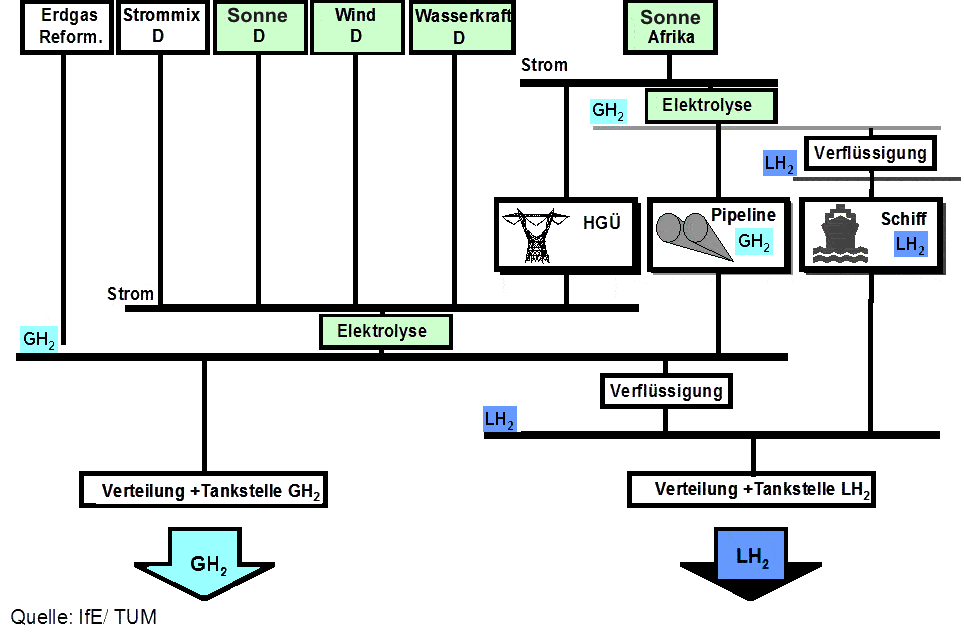
Wirklich umweltfreundlich ist die Brennstoffzelle deshalb nur, wenn man sie mit reinem Wasserstoff betreibt. Der benötigte Wasserstoff muss allerdings zuvor mit hohem Energieaufwand erzeugt werden. Idealerweise wird der Wasserstoff mit regenerativen Energien durch Elektrolyse aus Wasser hergestellt, was allerdings noch sehr teuer ist. Deshalb wird der in Brennstoffzellen eingesetzte Wasserstoff heute überwiegend aus fossilem Erdgas gewonnen. Wasserstoff wird als komprimiertes Gas (GH2) oder als Flüssigwasserstoff (LH2) bei tiefen Temperaturen zum Endverbraucher transportiert. Für ein flächendeckendes Netz einer Wasserstoffwirtschaft muss die nötige Infrastruktur entwickelt und ausgebaut werden (Pipelines, Hochdruck-Gasflaschen, Wasserstofftankstellen).
Hinweise
- Bei der Reformierung von Erdgas werden die Bestandteile Kohlendioxid und Methan weitgehend aus dem Erdgas entfernt, so dass das reformierte Gas zum überwiegenden Teil aus Wasserstoff besteht.
- HGÜ: Hochspannungs-Gleichstrom-Übertragung
- D: Gewinnung des Wasserstoffs in Deutschland
Einsatzmöglichkeiten
Brennstoffzellen können im Bereich kleiner Leistungen von einigen Watt für die Stromversorgung von Laptops oder Camcordern anstelle von Akkus eingesetzt werden. Brennstoffzellensysteme im kW Bereich wurden bereits für Automobile gebaut, deren Elektromotoren von den Brennstoffzellen versorgt werden.
Der Wasserstoff wird als Energieträger in Drucktanks oder in flüssiger Form in speziellen Tanks gespeichert. Stationäre Brennstoffzellensysteme im Leistungsbereich von einigen hundert kW bis zu 10 MW werden bereits als Kleinkraftwerke getestet, die neben elektrischer Energie auch die Abwärme als Nutzenergie einsetzen. Typische Einsatzmöglichkeiten dafür sind die zentrale Energieversorgung für Industrieanlagen, Einkaufszentren, Krankenhäuser oder auch Wohnsiedlungen.