Anmerkung: Im den folgenden Texten werden verschiedene Anwendungen vorgestellt, ohne diese in irgendeiner Form zu werten.
Diagnose durch Szintigraphie
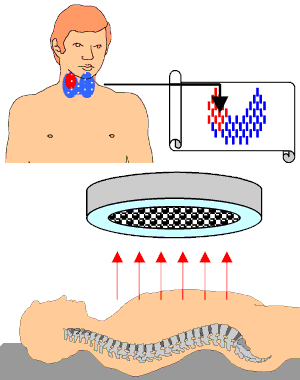
Bei der Szintigraphie (von Szintillation [lat.] = Flackern, Aufblitzen, Funkeln) wird ein sog. γ-strahlender Tracer intravenös in die Blutbahn des Patienten injiziert. Der Tracer verteilt sich anschließend im Körper seine Verteilung wird mit einem γ-Detektor aufgezeichnet. Für ein zweidimensionales Bild wird der Körper oder das untersuchte Organ zentimeterweise abgetastet und die Stärke der gemessenen γ-Strahlung als Helligkeits- oder Farbpunkt übertragen.
Heute nimmt man im Regelfall mit einem Computertomographen aus mehreren Richtungen auf und der Computer kann dann aus mehreren zweidimensionalen Bildern ein dreidimensionales Bild errechnen, das durch entsprechende Rechenoperationen in den verschiedensten Schnitten dargestellt werden kann.
Tracer-Isotope
Als Tracer dienen die in der Nuklearmedizin vor allem folgende radioaktive Isotope:
| 131J: | T½ = 8 d für Schilddrüsenuntersuchung; |
| 99Tc: | T½ = 6 h für Schilddrüsenuntersuchung und Skelettszintigraphie; das sehr kurzlebige 99Tc wird dabei durch Zerfall aus dem langlebigen 99Mo gewonnen. Man hat stets ausreichend von dem langlebigen 99Mo auf Lager und kann das nur kurz belastende 99Tc immer einsetzen. |
| 201Tl: | T½ = 73 h für Herzdurchblutungsuntersuchung; |
| 133Xe: | T½ = 5,3 d; |
| 18F: | T½ = 110 min (siehe hierzu PET) |
Früher erfolgte die Aufzeichnung durch einen sich zeilenförmig über dem Organ (hier Schilddrüse) bewegenden Szintillationszähler (Szintiscanner), der synchron die Messwerte als Strichmarkierung auf Papier übertrug. Moderne Gammakameras sind in der Lage, die γ-Strahlung eines Organs oder sogar des ganzen Körpers in einer einzigen Messung abzubilden.
Beispiele
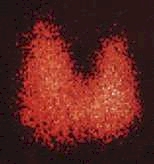
Schilddrüse (Abb. 3)
Die Schilddrüse speichert selektiv Jod für die Hormonsynthese. Injiziert man radioaktives Jod, wird dieses daher entsprechend der Stoffwechselaktivität angereichert und ist durch eine Gammakamera messbar. Nachteil der Radiojodszintigraphie ist trotz der unübertroffenen Aussagekraft eine relativ hohe Strahlenbelastung, so dass die Radiojodszintigraphie heute nur noch in der Tumordiagnostik und -therapie benutzt wird. Für diagnostische Routineuntersuchungen wird statt Radiojod daher 99Tc mit nur kurzer Halbwertszeit und sehr geringer Strahlenbelastung verwendet.
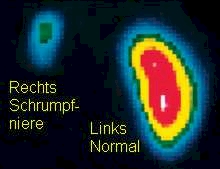
Niere (Abb. 4)
Nierenszintigramm; links Normalbefund, rechts Schrumpfniere. Als Tracer verwendet man radioaktive Substanzen, die von den Nieren stark ausgeschieden werden.
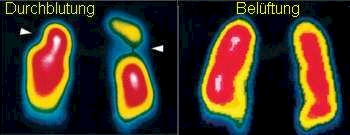
Lunge (Abb. 5)
Linkes Bild
Durchblutungsszintigraphie mit 99Tc-Injektion ins Blut (Perfusionsszintigramm): mehrere Durchblutungsdefekte in den Lungenspitzen (Pfeil).
Rechtes Bild
Belüftungsszintigraphie mit 133Xe in die Atemluft (Ventilationsszintigramm): Normalbefund; aus dem Unterschied beider Szintigramme ergibt sich die Diagnose Lungenembolie.
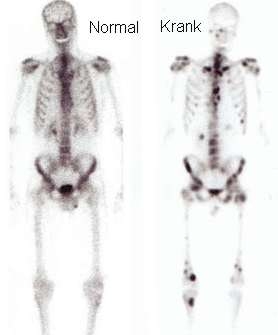
Knochen (Abb. 6)
Linkes Bild
Normales, also gesundes 99Tc-Skelettszintigramm.
Rechtes Bild
Skelettszintigramm mit zahlreichen Metastasen, also Tochtergeschwülsten eines Krebstumors.
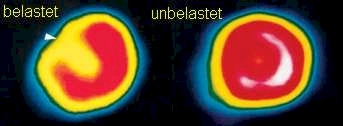
Herz (Abb. 7)
Linkes Bild
99Tc-Szintigramm des Herzens in Belastung (etwa auf dem Fahrradergometer): Der Pfeil weist auf eine gut sichtbare Mangeldurchblutung in der Vorderwand des Herzens.
Rechtes Bild
In Ruhe hat sich die Herzdurchblutung wieder normalisiert.
Quelle und weitere Information: http://www.nuklearmedizin.de, dort weiter unter Nuklearmedizin.
Positronen Emissions Tomographie (PET)
Bei der Positronen Emissions Tomographie (PET) werden radioaktiv markierte Substanzen (Tracer), die Positronen abstrahlen, in den Stoffwechsel eingeschleust und ihre Verteilung im menschlichen Körper mit einer PET-Kamera aufgezeichnet. Als Tracer kommen - in sehr geringen Mengen - Stoffe zum Einsatz, wie etwa Zucker, Eiweißbausteine, DNS-Bestandteile oder auch Wasser. Da diese markierten Substanzen im Körper weitgehend normal umgesetzt werden, ist mit der PET eine Darstellung der natürlichen Zellfunktionen - beispielsweise des Stoffwechsels oder der Proteinbiosynthese - möglich.
Ein bei der Krebsdiagnostik mit großem Erfolg eingesetzter Tracer ist das FDG (F18-Desoxyglukose), ein mit radioaktivem Fluor markiertes Traubenzuckermolekül. Das FDG wird bis zu einer bestimmten Stufe wie normaler Traubenzucker verstoffwechselt, der wiederum einer der Hauptbrennstoffe nahezu aller Zellen des menschlichen Körpers ist. In der Krebsdiagnostik mit FDG macht man sich zunutze, dass Krebszellen, deren Wachstum entreguliert ist, einen deutlich erhöhten Traubenzucker-Verbrauch gegenüber gesunden Zellen haben. Das FDG reichert sich also in den kranken, "entarteten" Zellen an. Im späteren PET-Bild hebt sich der Tumor dadurch ganz deutlich vom umliegenden, gesunden Gewebe ab. Schon Krebsabsiedlungen (Metastasen), deren Durchmesser nur wenige Millimeter betragen, können so erkannt werden.
Was ist das besondere an PET?
Bei Positronenstrahler macht man sich zunutze, dass das emittierte Positron im Gewebe schon bald nach seiner Emission auf ein ruhendes Elektron trifft und bei der Paarvernichtung zwei γ-Quanten mit jeweils der Ruheenergie eines Elektrons genau in entgegengesetzte Richtung abstrahlen.
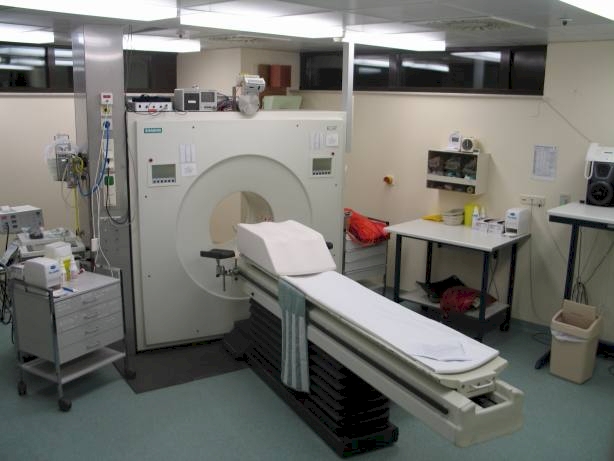
Diese Ereignisse werden von einer PET-Kamera entweder mit Hilfe eines Scannerringes, in dem der Patient liegt, oder mittels beweglicher Detektorköpfe, die um den Patienten kreisen, registriert. Die gleichzeitige Detektion der beiden Energieteilchen erlaubt es, die Linie, auf der der Zerfall stattgefunden hat, zu bestimmen. Aus der Überlagerung sehr vieler dieser Linien errechnet ein an die Kamera angeschlossener Computer schließlich ein komplexes Bild der Tracerverteilung im Körper des Patienten. Mit einer einzigen Untersuchung - der Patient wird schrittweise durch das Portal der PET-Kamera gefahren - kann so der gesamte Körper aufgenommen werden.
Diese paarweise Detektion der γ-Quanten führt zu einer gegenüber anderen nuklearmedizinischen Verfahren etwa 100fach höheren Empfindlichkeit und zu einer erhöhten Ortsauflösung.
Beispiele
Einsatz von PET bei der Onkologie (Krebsdiagnose und Behandlung)
- Suche nach dem Krebsherd und Feststellen der Bösartigkeit
- Bestimmung des Krankheitsstadiums
- Den Therapieerfolg rechtzeitig überprüfen
- Sicherheit nach der Krebsoperation
Bei diesem Patient, der nach überstandenem Schilddrüsenkrebs wieder erhöhte Tumormarker aufwies, konnte mit der PET - Aufnahme des Kopf-Hals-Bereiches eine Lymphknotenmetastase aufgespürt werden. Gut zu sehen ist, wie PET-Bilder (Mitte) mit Magnetresonanztomographieaufnahmen (oben) kombiniert werden können (unten), um den Tumor (im "Fadenkreuz") noch exakter zu lokalisieren.
Quelle und weitere Information: http://www.nuklearmedizin.de
Einsatz von PET in der Kardiologie (Herzkreislauferkrankungen)
- In der Vorfelddiagnostik (wie groß sind Nutzen und Risiko einer Bypass-Operation?)
- bei Durchblutungsstörungen bei einer koronaren Herzerkrankung
- für den frühen Nachweis einer Schädigung des Herzmuskels
- in der Herzinfarktdiagnostik
- vor Herztransplantationen
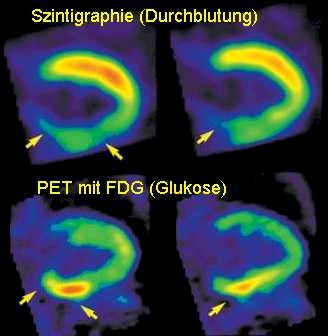
Bei einigen Fragestellungen der Kardiologie ist die Versorgung des Herzmuskelgewebes, dem Myokard, mit Nährstoffen von Bedeutung.
Die Bilder sind von einem 55jähriger Patient nach einem Herzinfarkt in der Hinterwand des Herzens. Oben wird mittels Myokardszintigraphie die Durchblutung des Herzmuskels dargestellt. Zu sehen ist die reduzierte Durchblutung der Hinterwand (gelbe Pfeile). Im unteren Bild wird mittels der FDG-PET der Stoffwechsel sichtbar gemacht. Deutlich ist zu sehen (gelbe Pfeile), dass gerade in den minderdurchbluteten Bereichen der Stoffwechsel erhöht ist. Hier spricht man von einer sogenannten Mismatch-Situation: Die beiden Befunde stimmen nicht überein. Dies spricht in diesem Fall für lebensfähiges, winterschlafendes Herzmuskelgewebe, das z.B. von einer Bypass-Operation profitieren würde.
Quelle und weitere Information: http://www.nuklearmedizin.de
Einsatz von PET in der Neurologie (Nervenerkrankungen)
- bei der Lokalisation des epileptogenen Fokus im Rahmen der präoperativen Epilepsiediagnostik
- in der frühen Diagnostik bei Parkinson´scher Erkrankung, degenerativen Multisystemerkrankungen und dem Veitstanz (Chorea Huntington)
- bei der Abgrenzung Depression-Demenz
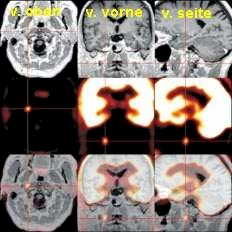
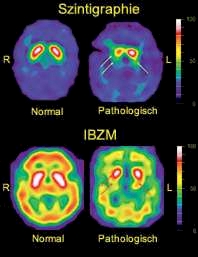
Die Bilder zeigen Untersuchungen des Gehirns(von unten) zur Feststellung der Parkinsonschen Krankheit und ihres Schweregrades.
Die oberen Bilder sind Szintigraphien, bei denen durch einen bestimmten Tracer der präsynaptischen Dopamin-Transporter (DAT) dargestellt wird, die unteren Bilder verdeutlichen die postsynaptischen Dopamin-D2-Rezeptoren durch einen entsprechenden Tracer (IBZM)
Quelle und weitere Information: http://www.nuklearmedizin.de.
Tumorbekämpfung durch Neutroneneinfang
Die Bor-Neutroneneinfang-Therapie befindet sich noch im Versuchsstadium. Wir verweisen an dieser Stelle auf den > Artikel bei Wikipedia.
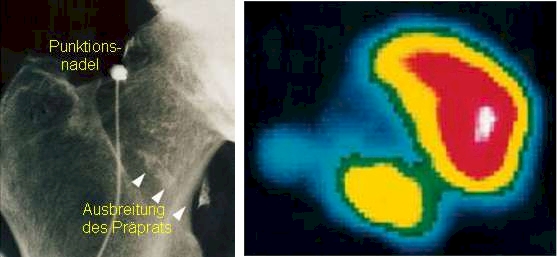
Rheumatherapie - Radiosynoviorthese
Rheumapatienten, bei denen einzelne Gelenke besonders schwer betroffen sind, können mit dem Verfahren der Radiosynoviorthese behandelt werden. Bei dieser nuklearmedizinischen Therapie wird ein Radiopharmakon direkt in das schmerzende, ruhiggestellte Gelenk gespritzt. Dort zerstört es die Zellen der wuchernden, entzündeten Gelenkinnenhaut (Synovia), die die Schmerzen verursacht. Zum Einsatz kommen dabei radioaktive Substanzen (Beta-Strahler), deren Strahlung im Gewebe nur eine Reichweite von wenigen Millimetern hat. Dadurch bleibt die Wirkung auf die entarteten Zellen der Gelenkinnenhaut beschränkt. Das umliegende Gewebe wird nicht geschädigt. Die Radiosynoviorthese kann, sollte die Gelenkinnenhaut erneut wuchern, problemlos wiederholt werden.
Quelle und weitere Information: http://www.nuklearmedizin.de; dort weiter unter Nuklearmedizin
Radioiodtherapie
Der größte Teil aller Schilddrüsentumoren leitet sich von normalem Schilddrüsengewebe ab und hat die Fähigkeit, Iod auch in der Form von radioaktivem Iod \({^{131}\rm{J}}\) zu speichern.
Schilddrüsenkrebszellen sind reichern aufgrund ihrer "Entartung" weniger Iod an als normales Schilddrüsengewebe. Die Speicherung von radioaktivem Iod in den Tumorzellen ist geringer als im normalen Schilddrüsengewebe. Darum erkennt man Tumore im Iod-Szintigramm als dunkle Flecken. Bei der Behandlung wird der Schilddrüsentumor und auch die gesamte normale Schilddrüse operativ entfernt. Der Chirurg entfernt bei der Operation - sofern vorhanden - auch vom Tumor befallene oder verdächtige Lymphknoten im Halsbereich.
Auch ein erfahrener Chirurg ist wegen der ansonsten zu befürchtenden Nebenwirkungen meist nicht in der Lage, die Schilddrüse wirklich komplett operativ zu entfernen. Aus diesem Grunde wird oft ca. 4 Wochen nach einer Schilddrüsenoperation eine Radioiodtherapie angesetzt.
Deren Aufgabe es ist, das nach der Operation verbliebene Schilddrüsenrestgewebe (und darin möglicherweise enthaltene Tumorzellen) auszuschalten. Radioaktives Iod wird von Schilddrüsengewebe und Schilddrüsenkarzinom-Zellen gespeichert, wobei die therapeutisch wirksamen β-Strahlen im Gewebe eine maximale Reichweite von 1 cm haben. Aufgrund dieser Tatsache und der sehr intensiven Anreicherung von radioaktivem Iod im Schildrüsenrestgewebe mit eventuell eingelagertem Tumorgewebe ist es möglich, mit der Radioiodbehandlung bei weitgehender Schonung des gesunden Gewebes sehr hohe Herddosen (Dosis im Resttumor oder in Tochtergeschwülsten) zu erzielen und damit die Tumorzellen abzutöten.
Radionuklidtherapie zur Schmerzlinderung
Patienten, die an Brust-, Prostata- oder Bronchialkrebs erkrankt entwickeln sehr häufig Knochenmetastasen, die oft zu sehr starken Schmerzen führen.
Neben der nur selten möglichen operativen Entfernung der Metastasen und der konventionellen, medikamentösen Schmerztherapie stellt die palliative (Lebensqualität verbessernde) Radionuklidtherapie eine nebenwirkungsarme, langanhaltende und für den Patienten wenig belastende Methode der Schmerzbekämpfung dar. Eine Heilung ist bei diesem Krankheitsbild im Regelfall nicht zu erwarten.
Zum Einsatz kommen dabei die Betastrahler \({^{186}\rm{Re}}\) und \({^{89}\rm{Sr}}\), die in den Blutkreislauf injiziert werden und sich überwiegend an das Skelett anlagern. Da der Knochenstoffwechsel in den Metastasen gegenüber dem gesunden Knochengewebe deutlich erhöht ist, wird in diesen "krankhaften" Bereichen deutlich am meisten Radionuklid "gebunden". Der übrige Teil des Radiopharmakons wird innerhalb von wenigen Stunden weitgehend über den Harn ausgeschieden.
Die schmerzlindernde Wirkung beginnt bei \({^{186}\rm{Re}}\) nach etwa 2 Tagen bei \({^{89}\rm{Sr}}\) nach ca. 2 Wochen und hält etwa 4 Wochen bis 12 Monate an und kann anschließend wiederholt werden.
Weitere Information findest du auf der Seite der Deutsche Gesellschaft für Nuklearmedizin.