Ernest RUTHERFORD untersuchte seit 1898 Alpha-Teilchen. Er war mit dieser neuartigen Strahlung völlig vertraut und konnte später auch nachweisen, dass es sich dabei um Helium-Kerne handelte. 1909 wurde er mit einer ziemlich unverständlichen Eigenschaft der Alphateilchen konfrontiert, auf die seine Schüler Hans GEIGER und Ernest MARSDEN bei Streuversuchen gestoßen waren.
GEIGER und MARSDEN beschossen 1909 eine sehr dünne Goldfolie mit einem eng begrenzten Strahl von Alphateilchen über mehrere Monate (sie führten diese Untersuchungen bis 1913 weiter). GEIGER verwendete eine Dicke von 8,6·10-6cm für die Folie. Tatsächlich war die Folie so dünn, dass sie auf ein Gitter aufgebracht wurde (bei dem Gitter ohne Folie wurden keine Reflexionen von Alphateilchen festgestellt, es war für Alphastrahlung durchsichtig).
Aufbau und Durchführung
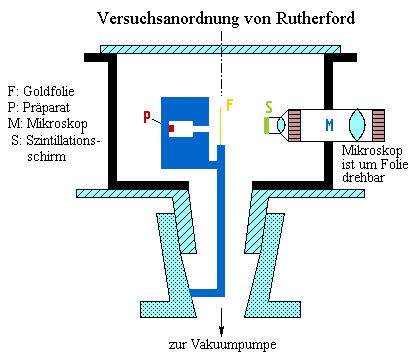
Ein radioaktives Präparat P befindet sich in einer Bleiummantelung, es sendet Alphateilchen aus, die auf eine sehr dünne Metallfolie (mehrere 1000 Atomlagen dick) treffen.
Die durchgehenden bzw. gestreuten Alphateilchen werden mit Hilfe eines Szintillationsschirms nachgewiesen. Dieser leuchtet kurzzeitig an der Stelle auf, wo er von einem Alphateilchen getroffen wird.
Zur genauen Lokalisation dient das Mikroskop, welches hinter dem Szintillationsschirm angeordnet ist. Das Mikroskop samt Szintillationsschirm kann um die Goldfolie gedreht werden.
Die Zählrate ΔN der in einer bestimmten Zeiteinheit auf den Schirm treffenden Alphateilchen wird in Abhängigkeit vom Drehwinkel \(\vartheta \) (Ablenkwinkel der Alphateilchen) bestimmt.


Abb. 2 zeigt vorne den Druckdeckel, seitlich hinten die Vakuumanschlüsse und der Einschusskanal für schnelle Teilchen aus einem Beschleuniger und oben die Registriergeräte (drehbar)
Erwartete Beobachtung
Zum Zeitpunkt der Durchführung des Experiments von GEIGER und MARSDEN war bereits bekannt, dass das Atom einen Radius von etwa \(10^{-10}\,\rm{m}\) hat, sich in ihm negativ geladene Elektronen befinden und es nach außen elektrisch neutral ist und somit auch eine positive Ladung beinhalten muss. Beim damals vorherrschenden THOMSONschen Modell (auch Wassermelonenmodell oder Rosinenkuchenmodell genannt) sollte sich die ganze Atommasse homogen auf den Raum verteilen, den das Atom in Anspruch nahm.
Nach diesem Modell müssten alle Alphateilchen ungehindert durch die Atome der Goldfolie dringen und alle auf der gegenüberliegenden Seite des Alpha-Strahlers ankommen. Dieses Verhalten stellt die Animation in Abb. 4 schematisch dar.
Tatsächlich gemachte Beobachtungen
Die Formulierungen der Beobachtungen sind angelehnt an die Originalarbeit von 1911.
1.Nahezu alle Alphateilchen gingen durch die Goldfolie hindurch, so als wäre sie nicht da. Diese Alphateilchen bewegten sich geradlinig weiter, bis sie auf die Wand oder den Detektor aufschlugen.
2.Einige wenige Alphateilchen wurden geringfügig abgelenkt, üblicherweise um einen Winkel von 2° und weniger. GEIGER fand heraus, dass ein Alphateilchen im Durchschnitt an einem Goldatom um \(0{,}005^\circ \) abgelenkt wird. Die wahrscheinlichste Ablenkung an der ganzen Goldfolie lag unter einem Grad (RUTHERFORD benannte sie in seiner Veröffentlichung von 1911 mit \(0{,}87^\circ \)).
3.Ganz wenige Teilchen wurden um einen Winkel von mehr als \(90^\circ \) abgelenkt. (1 von 8000 bei einer Platinfolie, RUTHERFORD nannte in seiner Veröffentlichung von 1911, dass es 1 von 20 000 bei der verwendeten Goldfolie sind). Dieses Ergebnis veranlasste RUTHERFORD zu der oft zitierten Aussage:
"Es war bestimmt das unglaublichste Ergebnis, das mir je in meinem Leben widerfuhr. Es war fast so unglaublich, als wenn einer eine 15-Zoll-Granate auf ein Stück Seidenpapier abgefeuert hätte und diese zurückgekommen wäre und ihn getroffen hätte."
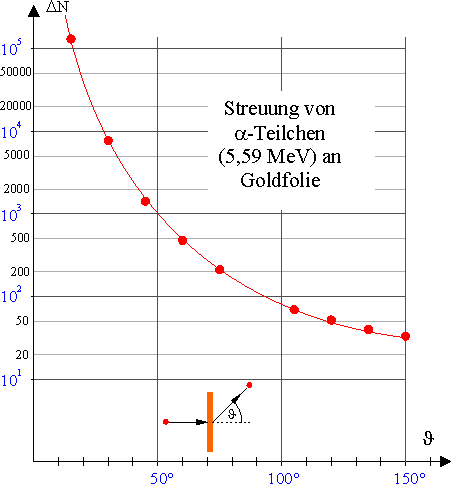
Teilchenzahl unter verschiedenen Streuwinkeln
Das Diagramm in Abb. 6 zeigt den Zusammenhang zwischen dem Ablenkwinkel \(\vartheta \) und der Anzahl \(\Delta N\) der in einen bestimmten Raum- und Zeitbereich gestreuten Alphateilchen. Beachte, dass es sich bei der y-Achse um keinen linearen Maßstab handelt.
Das Diagramm zeigt, dass der größte Teil der auf die Folie treffenden Alphateilchen die Folie nahezu unabgelenkt passieren konnte. Es kommen aber sehr selten auch Streuungen mit Streuwinkeln größer als 90° vor.
Hinweis: Die Erklärung der Großwinkelstreuung als Folge mehrerer hintereinander erfolgten Kleinwinkelstreuungen an verschiedenen Goldkernen ist nicht haltbar, da es aufgrund der sehr dünnen Folie unwahrscheinlich ist, dass ein Alphateilchen beim Durchdringen der Folie sehr nah an mehreren Kernen vorbeifliegt.
Erklärung von Rutherford
Die Beobachtung der stark abgelenkten Alphateilchen konnte mit dem Atommodell von THOMSON nicht erklärt werden.
RUTHERFORDs Lösung des Problems der Erklärung von der Streuung der Alphateilchen an Goldatomen sowohl um kleine als auch um große Winkel lag im Atomkern. RUTHERFORD erklärte, dass die ganze Atommasse im Zentrum des Atoms auf einem sehr kleinen Raum vereinigt sei. Dies nannte er den Atomkern.
In seiner Veröffentlichung von 1911 schlug er vor, den Kern als einen Punkt zu betrachten: "Wir müssen uns die Masse und die positive Ladung sowohl des Atoms als auch des Alphateilchens in einem Punkt konzentriert vorstellen, dessen Ausmessungen weniger als \(10^{-14}\,\rm{m}\) sind." RUTHERFORD verwendete in seiner Veröffentlichung nicht das Wort "Kern". Er nannte es "Ladungskonzentration". In einem Artikel von 1912 schrieb er einige Seiten über das Atommodell und verwendete dort erstmals das Wort "Kern".
Hinweise:
- Am Anfang seiner Überlegungen legte sich Rutherford zunächst noch gar nicht über das Vorzeichen der Ladung des Kerns fest. Er sprach nur von einer "zentralen Ladung".
- Später legte er sich auf eine positive Zentralladung fest: ". . .an atom having a positive central charge N·e, and surrounded by a compensating charge of N electrons . . . "
Erläuterung des Experimentes mit dem Rutherfordschen Atommodell
Die Animation in Abb. 8 zeigt die moderne (Atomkern aus positiv geladenen Protonen und elektrisch neutralen Neutronen) Erklärung des Streuexperiments von GEIGER und MARSDEN: Diejenigen Alphateilchen, die weit genug von Kernen entfernt die Folie durchdringen, werden so gut wie nicht abgelenkt. Nur die wenigen Geschosse, welche sehr nahe an einem Kern vorbeifliegen, erfahren eine nennenswerte Ablenkung. Dabei gilt: Je kleiner der Abstand zum Kern, desto größer der Streuwinkel.
Insgesamt erklärt das Atommodell von RUTHERFORD mit dem Atomkern die drei wesentlichen Ergebnisse des Experiments von GEIGER und MARSDEN:
1.Der Kern ist so klein, dass sich die überwältigende Mehrheit aller Alphateilchen ohne jegliche Ablenkung durch die Goldfolie hindurchbewegt, als wäre dort nichts. Es sieht so aus als wäre das Atom ein hauptsächlich leerer Raum. Die Wechselwirkung der geladenen Alphateilchen mit den Hüllenelektronen führt wegen der relativ hohen kinetischen Energie der Alphateilchen und der im Vergleich zu den Elektronen viel größeren Masse zu keiner nennenswerten Ablenkung.
2.Nur einige Alphateilchen gelangen beim Durchgang durch die Folie so nahe an einen Atomkern, dass die elektrische Abstoßung der beiden positiv geladenen Körperchen zu einer geringfügigen Ablenkung des Alphateilchens um ein oder zwei Grad führt. Die Wahrscheinlichkeit für diese Nähe zum Kern und die daraus resultierende Ablenkung wurden durch RUTHERFORD und seine Mitarbeiter berechnet und mit den Versuchsergebnissen verglichen. Es gab eine sehr gute Übereinstimmung.
3.Nur ganz wenige Alphateilchen treffen fast direkt auf die Mitte des Atoms. Die Alphateilchen, die sich mit etwa 10 % der Lichtgeschwindigkeit dem Atomkern nähern, werden durch dessen elektrische Kräfte vollelastisch "reflektiert". Da das Alphateilchen wesentlich leichter als der Goldkern ist, wird es auf einer hyperbelförmigen Bahn "reflektiert", so dass es um einen Winkel von 90° und mehr abgelenkt wird. Der Kern nimmt bei diesem Stoß nur geringfügig Energie von den Alphateilchen auf, die aber nicht ausreicht, um das Atom aus dem Metallverbund zu lösen.

